Haberler
Gıda Mikrobiyolojisinde Metot Validasyonu
Metot validasyonu terimi, bir metodun kullanım amacına uygunluğunun objektif kriterler ile teyit edilmesi olarak tanımlanabilir.
02 Aralık 2015, Çarşamba

Yrd. Doç. Dr. Emrah TORLAK
Konya Üniversitesi
Fen Fakültesi
Gıda mikrobiyolojisinde metot validasyonu, genellikle analiz sürelerini kısaltmak amacı ile geliştirilen alternatif metotların referans metotlar ile eşdeğer olduğunun teyit edilmesidir. Gıdaların mikrobiyolojik analizlerine yönelik referans metotlar ulusal (TSE, NEN vs) ve uluslararası (ISO, IDF vs) organizasyonlar tarafından yayınlanan klasik kültürel metotlardır. Referans metot kavramı gıda mikrobiyolojisinde olduğu gibi analiz sonuçlarının doğrudan analitik prosedüre dayalı olduğu analizler için geçerlidir.
Gıda endüstrisinde analiz sonuçlarının hızlı elde edilmesi mikrobiyolojik gıda güvenliği risklerine karşı önlemlerin zamanında alınabilmesi için bir gerekliliktir. Bu nedenle immunoassay, impedimetre, flow sitometri, nükleik asit hibridizasyon ve biyolüminesans gibi klasik kültürel metotlardan farklı analitik prensiplere dayalı birçok alternatif hızlı metot laboratuvarların kullanımına sunulmuştur. Bu alternatif metotların validasyonu üretici firmaların talebi ve finansmanı ile bağımsız organizasyonlar tarafından (AOAC, AFNOR, MicroVal, NordVal vs) ilgili ISO standardı (ISO 16140) veya bu organizasyonlarca yayınlanan validasyon rehberlerine göre gerçekleştirilmektedir. Alternatif metotlar, kalitatif veya kantitatif olmalarına bağlı olarak farklı performans karakteristikleri ile değerlendirilirler.
ISO/IEC 17025 standardına göre gıda mikrobiyolojisi laboratuvarları referans metotları veya validasyon çalışmaları gerçekleştirilmiş alternatif metotları tercih ettiklerinde yalnızca metodu uygulamada ki yeterliliğin değerlendirilmesine yönelik verifikasyon çalışmalarını gerçekleştirmekten sorumludurlar. Yani metot verifikasyonu metodun değil laboratuvarın yeterliliğine yöneliktir. Bu nedenle sekonder validasyon veya kısıtlı validasyon olarak ta isimlendirilmektedir.
Kantitatif mikrobiyolojik metotların verifikasyonu amacıyla iki performans karakteristiği değerlendirilmelidir; doğruluk (Trueness) ve kesinlik (Precision). Elde edilen analiz sonuçlarının doğru kabul edilen değere yakınlığı olarak ifade edebileceğimiz doğruluk yeterlilik testlerinden elde edilen sonuçlar veya kontamine edilen örneklerden elde edilen geri kazanım (Recovery) değerleri ile değerlendirilebilir. Aynı örnekten elde edilen analiz sonuçlarının birbirine yakınlığı olarak ifade edebileceğimiz kesinlik ise sabit veya farklı koşullar altında değerlendirilebilir. Koşulların (Analist, zaman, ekipman) sabit olduğu çalışma tekrarlanabilirlik (Repeatability), farklı olduğu çalışma ise laboratuvar içi tekrarüretilebilirlik (Intra-lab reproducibility) olarak isimlendirilir. Mikrobiyolojinin doğası gereği bu koşullardan zamanın değiştirilmesi mümkün değildir. Bu durumda personel ve mümkün olduğu sürece ekipman değişikliği ile laboratuvar içi tekrarüretilebilirlik şartları sağlanabilir.
ISO/TS 19036 standardı gıda mikrobiyolojisi analizlerinde laboratuvar içi tekrarüretilebilirliğin değerlendirilmesi için pratik bir protokol tanımlamıştır. Aynı protokol ISO 5725-3 standardında laboratuvar içi tekrarüretilebilirliğin değerlendirilmesi için alternatif yöntem olarak yer almaktadır. Bu protokolün kullanılması durumunda elde edilen standart sapma ölçüm belirsizliğinin hesaplanmasında kullanılabilir. Ölçüm belirsizliği, ölçülen büyüklüğün gerçek değerini içinde bulunduran değerler aralığını karakterize eden tahmini değerdir ve sayısal bir değer olarak yalnızca kantitatif analizler için geçerlidir. Gıda mikrobiyolojisi laboratuvarları verifikasyon ve kalite kontrol çalışmalarından elde edilmiş yeterli kesinlik verilerine sahip olmaları durumunda ölçüm belirsizliklerin yalnızca bu verileri kullanarak hesaplayabilirler. Mikrobiyolojik analizlerde birçok belirsizlik kaynağı için belirsizliğin hesaplanmasının mümkün olmaması nedeni ile GUM (ISO/IEC 98-3, Guide to the expression of uncertainty in measurement) prensiplerinin kullanılması mümkün değildir. Laboratuvar içi tekrarüretilebilirlik çalışmasından elde edilen standart sapma muhtemel belirsizlik kaynaklarını kapsamasından dolayı birleştirilmiş belirsizlik olarak kabul edilebilir.
Kalitatif metotların verifikasyonu amacıyla hassasiyet (Sensitivity) değerlendirilmelidir ve bu amaçla düşük düzeyde kontamine edilen (Örneğin, 5-10 kob/25 g) örnekler kullanılmalıdır. Poisson dağılım prensibinden dolayı hedef kontaminasyon düzeyinin 5 kob/25 g’ ın altında olması durumunda analize aldığımız örnek hedef bakteriyi içermeyebilir. Bu durumda negatif sonuçların yorumlanması problem olacaktır.
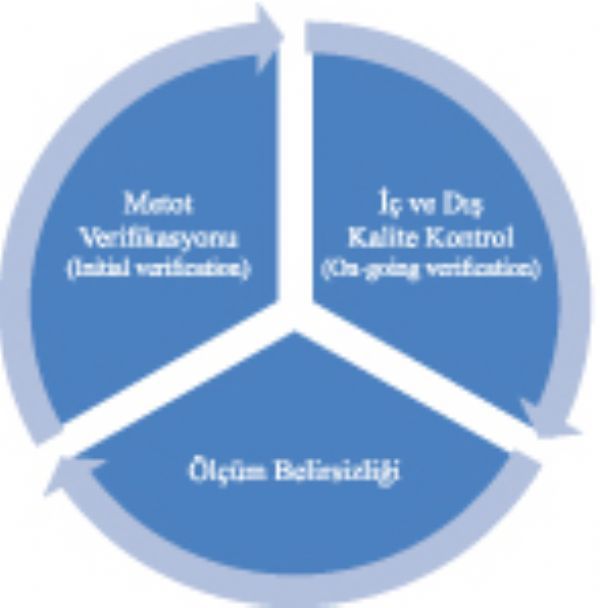
Metot verifikasyonu ve iç/dış kalite kontrol birbirlerini tamamlayan kavramlardır. Bu nedenle bazı kaynaklarda iç ve dış kalite kontrol çalışmaları devam eden verifikasyon (On-going verification) olarak tanımlanmıştır. Gıda mikrobiyolojisi laboratuvarları iç kalite kontrol amacıyla kantitatif analizler için doğruluk ve kesinliği, kalitatif analizler için ise hassasiyeti değerlendirmelidirler. Kantitatif analizler için doğruluk bir dış kalite kontrol yöntemi olan yeterlilik testleri ile değerlendirilmektedir. Bu nedenle kesinlik, kantitatif mikrobiyolojik analizlere yönelik iç kalite kontrol için bir zorunluluktur. Aynı örnekten elde edilen iki analiz sonucu arasındaki farkın belirlenen limit değerler ile karşılaştırılması kesinliğe yönelik en pratik iç kalite kontrol çalışması olacaktır. Kontrol örneği ISO/TS 19036 standardında tanımlanan protokole göre çalışıldığı takdirde limit değer olarak verifikasyon çalışmalarında elde edilen laboratuvar içi tekrarüretilebilirlik limiti (SR×2,83) kullanılabilir. İç kalite kontrol çalışmaları sayesinde laboratuvarlar gerektiğinde ölçüm belirsizliklerinin yeniden hesaplanması için her zaman güncel kesinlik verilerine sahip olacaklardır.
Bir laboratuvarda metot ile verilen faktörlerde değişiklikler kaçınılmazdır. Bu değişiklere farklı marka besiyeri veya biyokimyasal kit kullanımı, klasik doğrulama testleri yerine biyokimyasal kit kullanımı, farklı marka veya model inkübatör kullanımı veya manual koloni sayımı yerine otomotize sistemlerin kullanılmasını örnek verebiliriz. Bu örneklere daha birçok faktördeki değişiklikleri ilave edebiliriz. Metot faktörlerinde her bir değişiklik sonrasında verifikasyon çalışmalarının tekrarı gerekli midir? ISO/IEC 17025 standardının teknik şartlarına yönelik prosedürlere sahip laboratuvarlar için bu sorunun cevabı hayır olacaktır. Tüm bu faktörler için gerekli kontrol çalışmaları ISO/IEC 17025 standardında ve ilgili EA rehber dokümanında (04/10) metot verifikasyonundan farklı başlıklar altında tanımlanmıştır. Akreditasyonun gereği olarak gıda mikrobiyolojisi laboratuvarları besiyerleri, biyokimyasal kitler ve cihazlara yönelik kalite kontrol faaliyetleri ile bu faktörlerin uygunluğunu, iç ve dış kalite kontrol faaliyetleri ile bu faktörlerdeki değişiklerin analiz sonuçlarına etkisini düzenli olarak değerlendirmelidirler. Kontrol programlarına sahip laboratuvarlar için besiyeri ve cihaz gibi metot faktörlerindeki değişiklikler akreditasyon açısından engel değildir ve metot verifikasyon çalışmalarının tekrarını gerektirmez.
Kaynaklar
AOAC INTERNATIONAL BPMM Task Force Final Report 8-7-06, 2006, Presidential task force on best practices for microbiological methodology.
EA 04/10, 2002, Accreditation for Microbiological Laboratories.
ISO 16140, 2003, Microbiology of food and animal feeding stuffs - Protocol for the validation of alternative methods.
ISO 5725-3, 1994, Accuracy (trueness and precision) of measurement methods and results - Part 3: Intermediate measures of the precision of a standard measurement method.
ISO/IEC 17025, 2005, General requirements for the competence of testing and calibration laboratories.
ISO/TS 19036, 2006, Microbiology of food and animal feeding stuffs - Guidelines for the estimation of measurement uncertainty for quantitative determinations.
RVA T2, 2006, Explanatory document on microbiology.